I sagen nævnes tre dødsfald
Lige nu læser andre
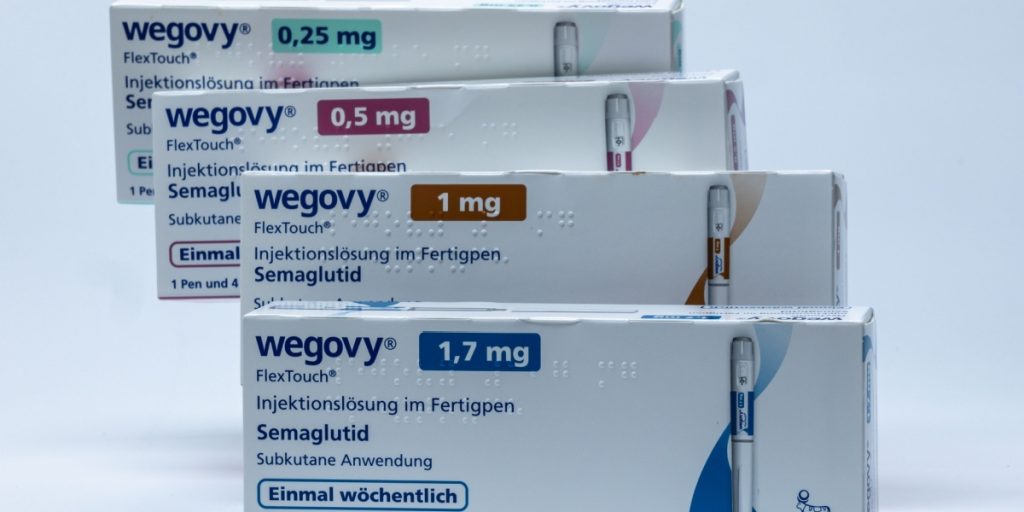
Vægttabsmedicin har på få år fået enorm opmærksomhed verden over.
Millioner af patienter bruger i dag præparater udviklet af danske Novo Nordisk, og interessen for midler som Ozempic og Wegovy er eksploderet.
Samtidig følger en voksende debat om mulige bivirkninger og hvordan de bliver registreret og indberettet til myndighederne.
Nu har netop det spørgsmål fået amerikanske sundhedsmyndigheder til at rette blikket mod medicinalgiganten.
Den amerikanske fødevare og lægemiddelstyrelse FDA har sendt et advarselsbrev til Novo Nordisk om selskabets procedurer for indberetning af mulige bivirkninger.
Læs også
Brevet blev sendt den 5. marts, skriver B.T.
Sagen handler om medicin, der indeholder stoffet semaglutid.
Det er det aktive stof i både diabetesmidlet Ozempic og vægttabsmidlet Wegovy.
Tre dødsfald
I brevet henviser myndigheden til tre dødsfald blandt patienter, som er blevet behandlet med medicin med semaglutid.
Ifølge oplysninger i sagen drejer et af dødsfaldene sig om et selvmord. Der nævnes også et tilfælde med selvmordstanker.
Læs også
FDA vurderer dog ikke, om dødsfaldene eller andre hændelser skyldes selve medicinen.
Advarslen handler i stedet om, hvorvidt Novo Nordisk har fulgt reglerne for indrapportering af potentielle bivirkninger.
Problemerne blev ifølge oplysninger opdaget under en inspektion på Novo Nordisks amerikanske hovedkontor i begyndelsen af 2025.
Kontoret ligger i Plainsboro i delstaten New Jersey.
Novo forventer løsning
Novo Nordisk bekræfter selv, at selskabet har modtaget brevet fra de amerikanske myndigheder.
Læs også
Ifølge virksomheden hænger sagen sammen med et inspektionsbesøg i februar sidste år.
Siden besøget har selskabet arbejdet på at håndtere de forhold, som myndigheden har rejst.
Novo Nordisk oplyser også, at man flere gange har orienteret FDA om fremdriften i arbejdet.
“Vi er sikre på, at vi vil løse de forhold, der er beskrevet i advarselsbrevet, til FDA’s fulde tilfredshed,” skriver Anna Windle, direktør for klinisk udvikling i Novo Nordisk i USA.
Ifølge selskabet er der allerede sendt flere tilbagemeldinger til de amerikanske myndigheder om de tiltag, der er sat i gang.